Para ilmuwan telah mempelajari
atom sejak ratusan tahun lalu. Para ilmuwan tersebut mengemukakan teori-teori
tentang atom. Teori yang satu akan runtuh atau ditolak ketika ada data atau
fakta baru yang ditemukan tentang atom sehingga melahirkan teori atom yang
baru. Berikut ini merupakan perkembangan teori atom.
1. John Dalton
 |
| Model Atom John Dalton |
Atom sebagai bola pejal dan merupakan bagian terkecil yang tidak dapat dibagi lagi. Setiap unsur terdiri atas atom-atom yang identik satu sama lain. Atom-atom dari unsur berbeda adalah berbeda. Atom-atom dapat bergabung membentuk molekul.
2. Joseph John Thomson
 |
| Model Atom Joseph John Thomson |
Atom merupakan bola bermuatan positif dan di tempat-tempat tertentu terdapat elektron-elektron yang bermuatan negatif, seperti kismis dalam roti.
3. Ernest Rutherford
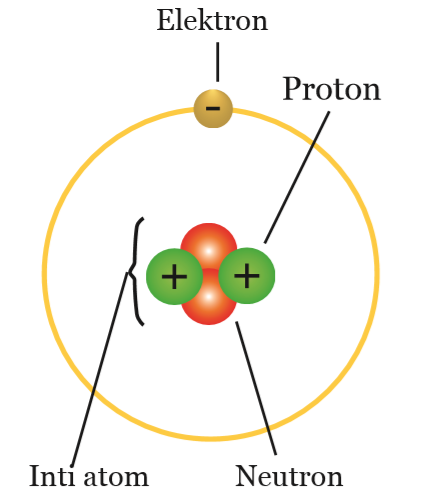 |
| Model Atom Ernest Rutherford |
Atom berbentuk bola yang di tengah-tengahnya terdapat inti atom yang merupakan pusat muatan positif dan pusat massa, sedangkan elektron-elektron bergerak berputar mengelilingi inti atom.
4. Niels Bohr
 |
| Model Atom Niels Bohr |
Atom terdiri atas inti atom yang menjadi pusat massa atom dan pusat muatan positif, sedangkan elektron bergerak mengelilingi inti atom pada lintasan tertentu (orbit) yang disebut kulit atom. Selama elektron bergerak mengelilingi inti pada orbitnya, elektron tidak memancarkan atau kehilangan energi.
5. Modern (Mekanika
Gelombang)
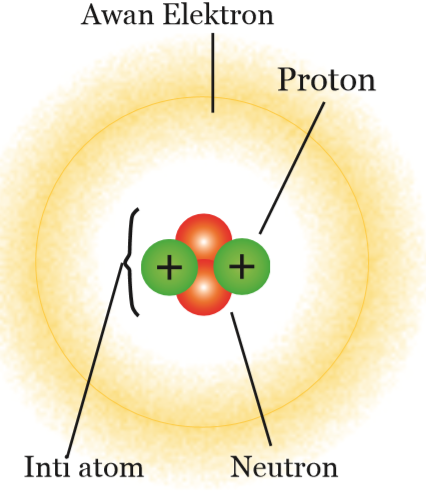 |
| Model Atom Modern (Mekanika Gelombang) |
Atom tersusun atas partikel subatom yaitu neutron (n), proton (p), dan elektron (e). Neutron dan proton membentuk inti yang padat, disebut nukleus atau inti atom. Elektron bergerak di sekeliling inti dengan kecepatan hampir seperti kecepatan cahaya dan membentuk awan elektron yang disebut orbital. Pada awan elektron tersebut posisi elektron tidak dapat ditentukan.
Teori atom yang paling baru adalah teori atom mekanika gelombang. Teori ini akan kamu pelajari ketika kamu menempuh pendidikan di Sekolah Menengah Atas. Berdasarkan teori atom Bohr dapatkah kamu menjelaskan bagaimana lampu yang berisi gas mulia yang berbeda dapat menghasilkan cahaya yang berwarna-warni? Begitu juga, bagaimana terbentuknya cahaya warna-warni dari kembang api?
Menurut Bohr, atom mempunyai
kulit-kulit atom tempat elektron bergerak mengelilingi inti atom. Kulit atom
yang paling dekat dengan inti atom mempunyai energi paling rendah. Kulit atom
yang lebih jauh dari inti atom mempunyai energi yang lebih tinggi. Elektron
yang berada pada kulit atom paling dalam dapat berpindah ke kulit atom yang
lebih luar bila menyerap energi dari luar atom. Energi itu dapat berasal dari
panas pembakaran atau dari energi listrik yang melewati atom-atom tersebut.
Elektron yang terletak pada kulit atom paling luar akan mendapatkan gaya tarik
yang lemah dari inti atom. Oleh karena itu elektron pada kulit atom paling
luar mudah lepas dari kulit itu, sehingga atom dapat kehilangan elektron. Bila
jumlah elektron dan jumlah proton dalam suatu atom tidak sama, atom tersebut
akan bermuatan atau menjadi ion. Proses pembentukan ion disebut ionisasi.
Tahukah kamu, elektron-elektron yang ada pada kulit atom paling luar mempunyai
peranan yang sangat penting pada pembentukan ikatan kimia antar atom dalam
suatu molekul?
Referensi:
Ilmu Pengetahuan Alam. SMP/MTs Kelas IX Semester 2. Kementerian Pendidikan dan Kebudayaan. Edisi Revisi Jakarta: Kementerian Pendidikan dan Kebudayaan, 2017
Baca juga:
Partikel Penyusun Benda dan Makhluk Hidup | |
01 | |
02 | |
03 | Mengidentifikasi Perbedaan Zat dalam Benda dan Makhluk Hidup |
04 | |
05 | |
06 | |
07 | |
08 | |
09 | |
10 | |
11 | |
12 | |
13 | |
14 | |
15 | |
16 | |
17 | Sifat Zat dan Hubungannya dengan Partikel Penyusun dan Strukturnya |
18 | |
19 | |
20 | |
Tidak ada komentar:
Posting Komentar